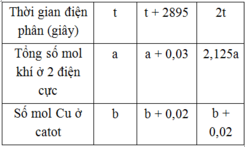
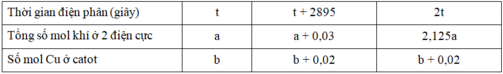
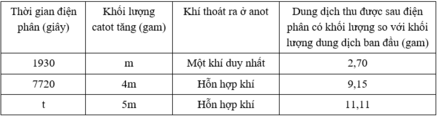
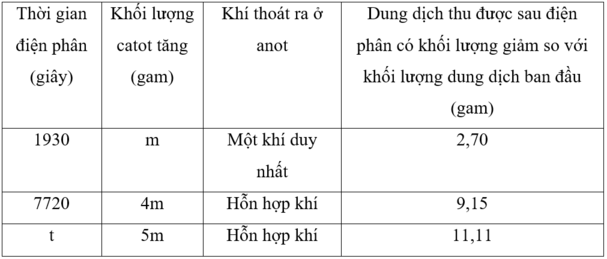
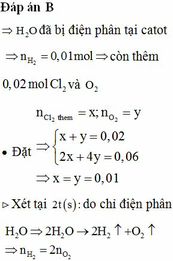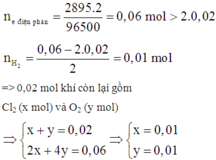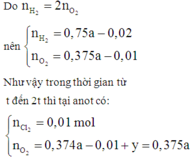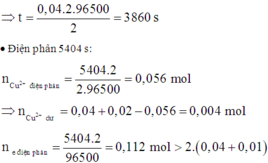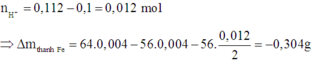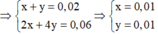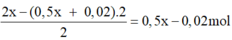Điện phân dung dịch chứa Cu(NO3)2, CuSO4 và NaCl với điện cực trơ, cường độ dòng điện không đổi 2A, hiệu suất 100%. Kết quả thí nghiệm được ghi trong bảng sau:
| Thời gian điện phân (giây) |
t |
t + 2895 |
2t |
| Tổng số mol khí ở 2 điện cực |
a |
a + 0,03 |
2,125a |
| Số mol Cu ở catot |
b |
b + 0,02 |
b + 0,02 |
Giá trị của t là
A. 4825
B. 3860
C. 2895
D. 5790